|
Гальваническая пара для источника питания
|
|
| | Сообщение # 1
|
gopik

Постов: 186
ОК |
ГАЛЬВАНИЧЕСКИЕ ЭЛЕМЕНТЫ: САМОДЕЛЬНАЯ БАТАРЕЯ
Живу в деревне, решил вот сделать себе какой нибудь источник питания, из доступных в деревне материалов. Остановился на алюминии (проволоки здесь полно, можно и листом разжиться) и на свинце (тоже можно с избытком найти под ногами).
Судя по электрохимическому ряду, эта пара должна выдавать в районе полтора вольта - что тоже вполне приемлимо. Сделал пробный элемент, да что то видать не пошло... Короче:
Отлил свинцовый штырь толщиной с палец (анод), обернул его несколькими слоями спандбонда чтобы не было контакта, и сверху намотал алюминиевую проволоку (катод). При опускании в ведро с водой выдаёт только 130 -150 милливольт. При деформации алюминиевой спирали - напряжение иногда подскакивает до 600мВ, но если оставить конструкцию в покое - то постепенно напруга падает до тех же 150мВ...
Видать собственных знаний в этом вопросе у меня недостаточно, в гугле - уже забанили, информации дохрена и мозг от неё закипает, а именно по такой паре металлов ничего не нашел... Почему то Вот решил обратится сюда за помощью в этом вопросе.
Может кто более сведующий в данном вопросе, подскажет что да как... Может электролит надо щелочной или кислотный,или вообще соль поваренную использовать? а может эта пара вообще не жизнеспособна изза каких-то особенностей этих металлов??? что я делаю не так?
Требования к источнику питания:
1. Размеры - не интерисуют, вес тоже, (земли хватает - можно закопать или поставить куда угодно)
2. Бюджетность (желательны материалы которые легкодоступны.. типа зола... соль...уксус...)
3. Долговечность (желательно чтобы элемент отрабатывал год другой, до необходимости замены катода)
4. По току - хотя бы чтоб 100мА мог держать 1 элемент
5. Ну и по напруге - если полтора вольта нереально, то пусть хотя-бы половину даст... или треть
У кого какие соображения или рекомендации будут по этой паре? может целесообразнее использовать железо... чугун... или другой хлам. заранее благодарен.
|
|
| | Сообщение # 2
|
Sam

Постов: 2341
U |
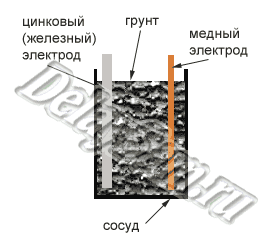
А при чём тут свинец и алюминий?Обычно работают с медью и цинком.Их достать в деревне не проблема, а по КПД ещё,наверное, и лучше даже будет.
|
|
| | Сообщение # 3
|
gopik

Постов: 186
ОК |
Цитата Sam (  ) А при чём тут свинец и алюминий?Обычно работают с медью и цинком.Их достать в деревне не проблема, а по КПД ещё,наверное, и лучше даже будет.
Ну... если так рассуждать - то лучше уж тогда медь и алюминий, эта пара не раз уже испытана, да там и выхлоп по напряжению побольше будет 
только вот ЦИНКА - я вообще в нашей деревне и в окрестностях ниразу не встречал... да и с медью проблемы (местные алкаши всё подбирают, разжиться конечно можно, но не в избытке и с техническими проблемами......) так что если бы было проще - то я бы и не спрашивал...
Так что хотелось бы услышать что нибудь конструктивное именно по паре СВИНЕЦ-АЛЮМИНИЙ |
|
| | Сообщение # 4
|
Sam

Постов: 2341
U |
Цитата gopik (  ) ЦИНКА - я вообще в нашей деревне и в окрестностях ни разу не встречал
Ни одной крыши из оцинковки нет что ли во всей деревне? |
|
| | Сообщение # 5
|
gopik

Постов: 186
ОК |
Цитата Sam (  ) Ни одной крыши из оцинковки нет что ли во всей деревне?
Во первых - НЕТ... во вторых - если присмотреться - то оцинковка это не ЦИНК... а всего лишь оцинкованное железо. надолго не хватит... и в третьих - даже если и найти такую крышу - то там люди живут. |
|
| | Сообщение # 6
|
nolpofaze

Постов: 442
Друзья |
gopik, я предполагаю, что ЭДС падает из-за алюминия, вернее его окисления. А оксид алюминия очень стойкая штука. Надо его чем то растворять, попробовать слабой органической кислотой (например уксус), ну и активный раствор использовать кислотный (тот же раствор уксуса).
Добавлено (29.05.2017, 13:16)
---------------------------------------------
В дополнение. Гальваническая пара это окислительно-восстановительная реакция. И в ней должны участвовать электроды из металлов которые расположены в электрохимическом ряду по разные стороны водорода т.о. для отрицательного полюса металлы до водорода, для положительного - после водорода.
Для твоей батарейки, если взять за отрицательный алюминий, то положительным дожны быть медь, ртуть, серебро, золото))) Хотя если сплав магний-алюминиевый то реакция будет и со свинцом.
|
|
| | Сообщение # 7
|
gopik

Постов: 186
ОК |
Провёл несколько экспериментов с разными растворами... везде лажа получается. Видать дело в оксидной плёнке на алюминии. Начитался так же про алюминий - Выводы не утешительные. Видать этот металл вообще негоже использовать если мы хотим сделать долгоиграющий источник питания. Есть конечно способы заставить его работать с помощью других электролитов, но нам этот способ не подходит... дюже дорогой.
Придётся рассмотреть другие пары.
пока всё еще рассматриваю тот же свинец... Но думаю рассмотреть железо...
в качестве плюсового электрода - пока решил поэкспериментировать с графитом... посмотрим что получится.
Положительный электрод у нас вроде как не окисляется? (ну в смысле не портится...) менять его не придётся?
|
|
| | Сообщение # 8
|
nolpofaze

Постов: 442
Друзья |
gopik, не окисляется, и даже должен восстанавливаться. В солевых батарейках применяется угольный стержень, только он в качестве токоотвода, а положительным электродом служит диоксид марганца в смеси с графитом и электролитом, отрицательный электрод - цинк. Так что положительный электрод все равно нужен и это нужен не графит....
Добавлено (30.05.2017, 12:28)
---------------------------------------------
Самый простой вариант, все-таки, медь(или сплавы с ее высоким содержанием) + железо, алюминий, цинк, олово...
Алюминий, кстати стоит левее цинка, если решить проблему с его оксидом, то пара медь-алюминий будет выдавать большую эдс.
Добавлено (30.05.2017, 13:06)
---------------------------------------------
А попробовать алюминий-медь и в качестве электролита - медный купорос...
|
|
| | Сообщение # 9
|
gopik

Постов: 186
ОК |
nolpofaze,
Не.. учитывая сложности с алюминием - даже неохота им заниматься... проблема с электролитом решаема - но ДОРОГО... проще соеденить последовательно несколько элементов...
Касательно графита: а если использовать МЕДНО-ГРАФИТНЫЙ стержень??? и вставить его например в обрезок 32й трубы... железо конечно будет быстро подвергаться коррозии, но благо металлолома в деревне хватает...
В качестве электролита - засыпать в эту трубу золу из печки, и позволить затекать туда атмосферным осадкам...
|
|
| | Сообщение # 10
|
nolpofaze

Постов: 442
Друзья |
Медный купорос вроде как и не проблема... А так можно экспериментировать и с золой, щелочь по сути. А может посмотреть не в сторону химического источника, попробовать генератор...?
|
|


